دوره 10، شماره 3 - ( پاییز 1402 )
جلد 10 شماره 3 صفحات 299-290 |
برگشت به فهرست نسخه ها
Research code: 990255
Ethics code: IR.MUMS.REC.1399.203
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Irandost A, Hajali V, Behnejad M, Payvar B, Khosravi Bonjar A, Bazazkahani H. Relationship Between the Results of Laboratory Tests, Lung CT Scan, and Real-time PCR in Suspected or Confirmed COVID-19 Patients in Quchan, Iran. J Prevent Med 2023; 10 (3) :290-299
URL: http://jpm.hums.ac.ir/article-1-672-fa.html
URL: http://jpm.hums.ac.ir/article-1-672-fa.html
ایران دوست امین، حاج علی وحید، به نژاد محبوبه، پایور بهاره، خسروی بنجار علی، بزازکاهانی حمید. بررسی معیارهای آزمایشگاهی و سیتیاسکن ریه با واکنش زنجیرهای پلیمراز همپا در بیماران مشکوک و قطعی کوویدـ19 در شهرستان قوچان: یک مطالعه گذشتهنگر. طب پیشگیری. 1402; 10 (3) :290-299
امین ایران دوست1 

 ، وحید حاج علی2
، وحید حاج علی2 

 ، محبوبه به نژاد3
، محبوبه به نژاد3 

 ، بهاره پایور4
، بهاره پایور4 

 ، علی خسروی بنجار5
، علی خسروی بنجار5 
 ، حمید بزازکاهانی*6
، حمید بزازکاهانی*6 




 ، وحید حاج علی2
، وحید حاج علی2 

 ، محبوبه به نژاد3
، محبوبه به نژاد3 

 ، بهاره پایور4
، بهاره پایور4 

 ، علی خسروی بنجار5
، علی خسروی بنجار5 
 ، حمید بزازکاهانی*6
، حمید بزازکاهانی*6 


1- گروه پرستاری، دانشکده پرستاری قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
2- گروه علوم اعصاب، دانشکده پرستاری قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
3- گروه بیماریهای عفونی و گرمسیری، بیمارستان موسی بن جعفر (ع) قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
4- گروه مراقبتهای ویژه پرستاری، دانشکده پرستاری قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
5- گروه پرستاری، مرکز مدیریت حوادث و فوریتهای پزشکی زابل، دانشگاه علوم پزشکی زابل، زابل، ایران.
6- گروه روانپرستاری، دانشکده پرستاری شیروان، دانشگاه علومپزشکی خراسان شمالی، بجنورد، ایران.
2- گروه علوم اعصاب، دانشکده پرستاری قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
3- گروه بیماریهای عفونی و گرمسیری، بیمارستان موسی بن جعفر (ع) قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
4- گروه مراقبتهای ویژه پرستاری، دانشکده پرستاری قوچان، دانشگاه علومپزشکی مشهد، مشهد، ایران.
5- گروه پرستاری، مرکز مدیریت حوادث و فوریتهای پزشکی زابل، دانشگاه علوم پزشکی زابل، زابل، ایران.
6- گروه روانپرستاری، دانشکده پرستاری شیروان، دانشگاه علومپزشکی خراسان شمالی، بجنورد، ایران.
متن کامل [PDF 3869 kb]
(603 دریافت)
| چکیده (HTML) (1534 مشاهده)
متن کامل: (787 مشاهده)
مقدمه
اخیراً شیوع ذاتالریه ویروسی (کوویدـ19) نگرانی جهانی را برانگیخته است. این ویروس برای اولینبار در دسامبر 2019 در استان ووهان چین گزارش شد و سپس بهسرعت در سایر نواحی چین منتشر شده و باعث یک اپیدمی بزرگ با تعداد 80894 مورد ابتلا شامل 3237 مورد مرگ تا هفدهم مارس 2020 شد [1]. در ایران بهطور رسمی در اواخر بهمن 1398 اولین موارد ابتلا به این ویروس اعلام شد که شامل 43 مورد ابتلا به همراه 8 مورد مرگ بود [2]. طبق آمار رسمی سایت سازمان بهداشت جهانی تا تاریخ 6 اکتبر 2022، برابر با 14 مهرماه 1401، تعداد کل موارد ابتلا در دنیا 625129794 مورد بوده است که از این تعداد 6556063 مورد جان خود را از دست دادهاند [3]. کروناویروس جدید با قدرت عفونتزایی بالا که بهطور رسمی Sever Acute Respiratory Syndrome Coronavirus2 و بهاختصارا SARSCoV-2 نامیده میشود، متعاقباً بهواسطه بررسی توالی ژنی و مطالعات اتیولوژیک بهعنوان عامل پاتوژن این شیوع گسترده معرفی شد [4 ,5]. باتوجهبه ماهیت عفونتزایی شدید این بیماری و فقدان استراتژیهای درمانی و دارویی اثباتشده و همچنین عدم کشف واکسن مؤثر تاکنون [6, 7] تشخیص سریع و قطعی در مراحل اولیه بروز بیماری از اهمیت حیاتی برخوردار است. تشخیص بیماری کوویدـ19 اساساً بر یافتههای آزمایشگاهی و رادیوگرافیک استوار است. در کل دنیا رادیولوژیستها با تشخیص کوویدـ19 نقش کلیدی در پیشبرد تشخیص و افتراق تظاهرات بالینی این بیماری از سایر یافتههای رادیولوژیک مشابه [8] و همچنین ارزیابی شدت و پیشرفت بیماری [9] دارند. البته روش تشخیصی اصلی که در بیشتر کشورها بهعنوان استاندارد طلایی تشخیصی محسوب میشود، واکنش زنجیرهای پلیمراز همپا بوده که RNA ویروس را شناسایی میکند [10]. تجربه کشورهای درگیر این بیماری حاکی از آن است که سیتیاسکن قفسه سینه میتواند با فراهم کردن جزئیات ویژه ظریف، نقش حیاتی در غربالگری و تشخیص پنومونی داشته باشد. مشخصه برجسته تصاویر رادیولوژیک در بیماران پنومونی در کوویدـ19 نمای شیشه مات و تراکم ریه است که میتواند هر 2 ریه را درگیر کند [8]. براساس تظاهرات بالینی نیز شایعترین علائم بیماری شامل تب، سرفه خشک، خستگی، تنفس کوتاه و سطحی، بیاشتهایی و اختلال در حس چشایی و ضایعات ریه در سیتیاسکن است. با وجود این در برخی از بیماران علائم و مشکلات شدید و حاد مربوط به پنومونی شامل سندرم زجر تنفسی حاد، ادم ریه، آسیب حاد کلیوی و یا نارسایی تعداد زیادی از ارگانهای بدن مشاهده میشود [11، 12].
علاوهبر سیتیاسکن و واکنش زنجیرهای پلیمراز همپا، آزمایشات خونی نظیر افزایش میزان CRP و LDH و همچنین تغییراتی در CBC نظیر لکوپنی یا لنفوسیتوپنی میتواند ما را به تشخیص قطعی نزدیکتر کنند [13]، اما باتوجهبه دوره کمون نامشخص و کاملاً متفاوت [14]، وجود افراد مبتلا به ویروس بدون علامت بالینی [15] و یا داشتن PCR منفی [16]، و علاوهبرآن باعنایت به وجود سیل زیاد اطلاعات رسمی و غیررسمی مبتنی بر پژوهش یا برخلاف آن براساس عقیده و نظر اثباتنشده، نیاز به توسعه و اتکای بر یافتههای مبتنی بر شواهد است تا به ارتقای کیفیت مراقبتهای بهداشتی و درمانی منجر شود [17] . بنابراین نیاز به بررسی بیشتر و مقایسه روشهای موجود و تعیین میزان همسویی بین روشهای رایج تشخیصی ازجمله سیتیاسکن واکنش زنجیرهای پلیمراز همپا و آزمایش خون است.
علی رغم مطالعات نسبتاً زیادی که درزمینه تظاهرات بالینی، رادیوگرافیک و آزمایشگاهی این بیماری تاکنون انجام شده است، مطالعات بسیار محدودی ارتباط بین تست اسمیر حلق، آزمایشگاهی و رادیولوژیک بیماران را مورد بررسی قرار دادهاند. بنابراین باتوجهبه اهمیت فوقحیاتی تشخیص سریع و قطعی این بیماری در درمان و میزان بقای بیماران، در این مطالعه بر آن شدیم تا با بررسی معیارهای آزمایشگاهی، سیتیاسکن ریه و واکنش زنجیرهای پلیمراز همپای بیماران مشکوک و قطعی کوویدـ19 در شهرستان قوچان، میزان تطابق نتایج روشهای روتین سهگانه با یکدیگر را در تشخیص بیماری بررسی کنیم.
مواد و روشها
پژوهش حاضر با کد اخلاق IR.MUMS.REC.1399.203 یک مطالعه گذشتهنگر است که بهمنظور تعیین معیارهای آزمایشگاهی و سیتیاسکن ریه با واکنش زنجیرهای پلیمراز همپا در بیماران مشکوک و قطعی کوویدـ19 در شهرستان قوچان انجام شد. به ملاحظات اخلاقی ازجمله حفظ محرمانگی افراد و گزارشدهی نتایج پژوهش بهصورت کلی توجه شد. جامعه پژوهش کلیه 400 بیمار مشکوک به کوویدـ19 مراجعهکننده به بیمارستان موسی بن جعفر (ع) از اول اسفند 1398 لغایت آخر اردیبهشت 1399 بود که برایشان آزمایش خون و یا سیتیاسکن ریه و بررسی واکنش زنجیرهای پلیمراز همپای حلق در بیمارستان انجام شد و سوابق و مستندات آن موجود است. روش نمونهگیری، بهصورت سرشماری و براساس معیارهای ورود و خروج صورت گرفت. معیارهای ورود به مطالعه: 1. ورود و بستری در بیمارستان با احتمال یا داشتن علائم کرونا و شروع پروسه درمان کوویدـ19 توسط متخصص داخلی یا عفونی؛ 2. انجام هر 3 اقدام پاراکلینیکی (آزمایش خون و سیتیاسکن ریه و واکنش زنجیرهای پلیمراز همپای حلق) برای بیمار در بیمارستان و وجود سوابق و مستندات در بایگانی بیمارستان.
پس از اخذ تاییدیه و کد اخلاق از دانشگاه علومپزشکی مشهد و اخذ اجازه کتبی از مدیریت شبکه بهداشت و درمان قوچان، با مراجعه به بایگانی اسناد بیمارستان، آزمایشگاه و واحد سیتیاسکن بیمارستان، اطلاعات موردنیاز و از قبل مشخصشده که شامل 5 آیتم آزمایشگاهی (WBC – LYMPHOCIT – CRP – LDH – ESR)، ریپورت مکتوب سیتیاسکن ریه توسط رادیولوژیست و نتیجه تست واکنش زنجیرهای پلیمراز همپای حلق موجود در پرونده بیمار بود، ثبت شد.
به این منظور پژوهشگر باسابقه (کارشناس پرستاری)، بهصورت شبانهروزی و در تمام روزهای هفته به بیمارستان موسی بن جعفر (ع) قوچان مراجعه کرد و پرونده تمام بیماران مراجعهکننده (دارای پرونده) را که تشخیص اولیه آنها کوویدـ19 بود (روش سرشماری) را مورد مطالعه قرار داد و اطلاعات خواستهشده را خارج کرد. از حدود 400 نفر اولیه، کسانی که فاقد معیارهای ورود بودند از لیست خارج، و نهایتاً 221 نفر وارد مطالعه شدند و اطلاعات آنها برای تجزیهوتحلیل تحویل کارشناس آمار شد.
ابزار گردآوری دادهها عبارت بود از فرم ساده طراحیشده جهت ورود دادههای ثبتی پرونده بیماران (بستری در بیمارستان موسی بن جعفر (ع) قوچان بهعنوان تنها مرکز پذیرش بیماران کوویدـ19 در شهرستان قوچان)، شامل سن، جنس، نتیجه آزمایشات پنجگانه خون که در مرحله بعد براساس استانداردهای موجود و توسط متخصص عفونی (فوکال پوینت کرونا) بهصورت منفی، مثبت یا مشکوک گزارش میشد؛ گزارش سیتیاسکن ریه توسط رادیولوژیست بهصورت مثبت، منفی یا مشکوک و جواب آزمایش واکنش زنجیرهای پلیمراز همپا بهصورت مثبت یا منفی. نهایتاً دادهها با استفاده از آمار توصیفی و استنباطی، ازجمله آزمون کایاسکوئر و آماره وی کرامر در نرمافزار SPSS نسخه 19 مورد تجزیهوتحلیل قرار گرفت.
یافتهها
میانگین سنی افراد 11/4±60 سال بود. 48/2 درصد مرد و 51/58 درصد از بیماران زن بودند. متغیرهای موردمطالعه ما، نتایج آزمایش واکنش زنجیرهای پلیمراز همپای حلق، نتایج سیتیاسکن ریه و تشخیص پزشک متخصص عفونی براساس نتایج آزمایشات پنجگانه خون است. جدول شماره 1 فراوانی و درصد نتایج 3 متغیر ذکرشده را نشان میدهد.

جدول شماره 2 که شامل جداول توافقی بین سیتیاسکن ـ واکنش زنجیرهای پلیمراز همپا، آزمایش خون ـ واکنش زنجیرهای پلیمراز همپا و آزمایش خون ـ سیتیاسکن است، میزان همسویی بین گزارش رادیولوژیست از سیتیاسکن و نتایج واکنش زنجیرهای پلیمراز همپا، ارتباط بین آزمایش خون و نتایج واکنش زنجیرهای پلیمراز همپا و ارتباط بین آزمایش خون و نتایج سیتیاسکن را نشان میدهد.
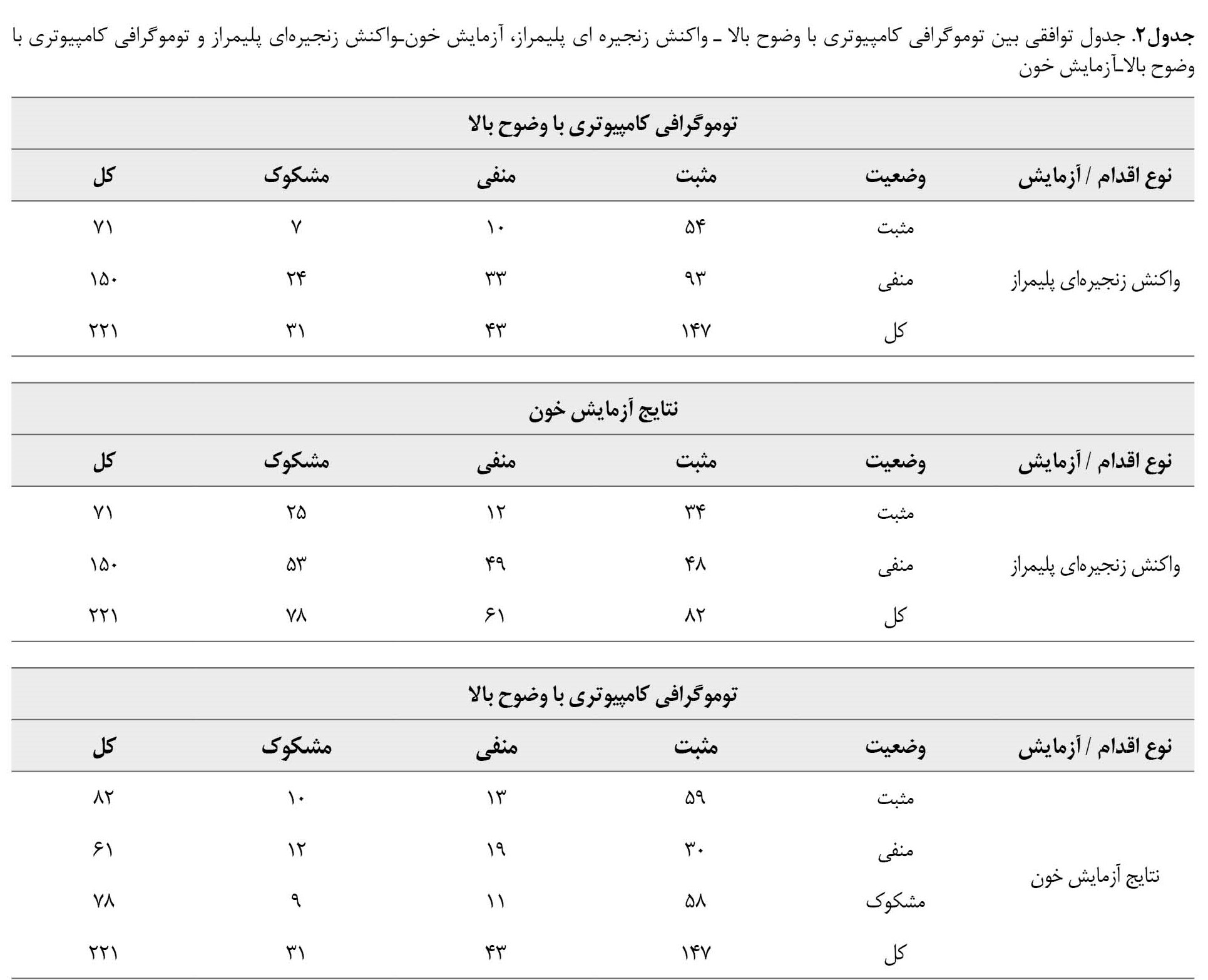
براساس نتایج جدول به نظر میرسد بیشتر افراد با واکنش زنجیرهای پلیمراز همپای مثبت، نتیجه سیتیاسکن مثبت هم داشتهاند (76 درصد). گرچه معنادار بودن این مسئله، با استفاده از آزمون کایاسکوئر و نتایج آن (P=0/118)، رد شد. همچنین به نظر میرسد تعدادی از افراد که نتیجه واکنش زنجیرهای پلیمراز همپای مثبت داشتهاند، دارای آزمایش خون مثبت بودهاند (47/8 درصد) که معنادار بودن این مسئله نیز با استفاده از آزمون کایاسکوئر (P=0/02)، تأیید شد و میزان رابطه این 2 متغیر با آماره وی کرامر 0/186 به دست آمد. علاوهبراین یافتهها نشان میدهند بیشتر افراد با نتیجه آزمایش خون مثبت، نتیجه سیتیاسکن مثبت هم داشتهاند (71/9 درصد). معنادار بودن این مسئله نیز با استفاده از آزمون کایاسکوئر (P=0/019)، تأیید شده و میزان رابطه این 2 متغیر در 3 سطح، با آماره وی کرامر 0/231 به دست آمد.
درنهایت جدول شماره 3 نتایج منفی و مثبت هر 3 تست تشخیصی را در کنار هم نشان میدهد.
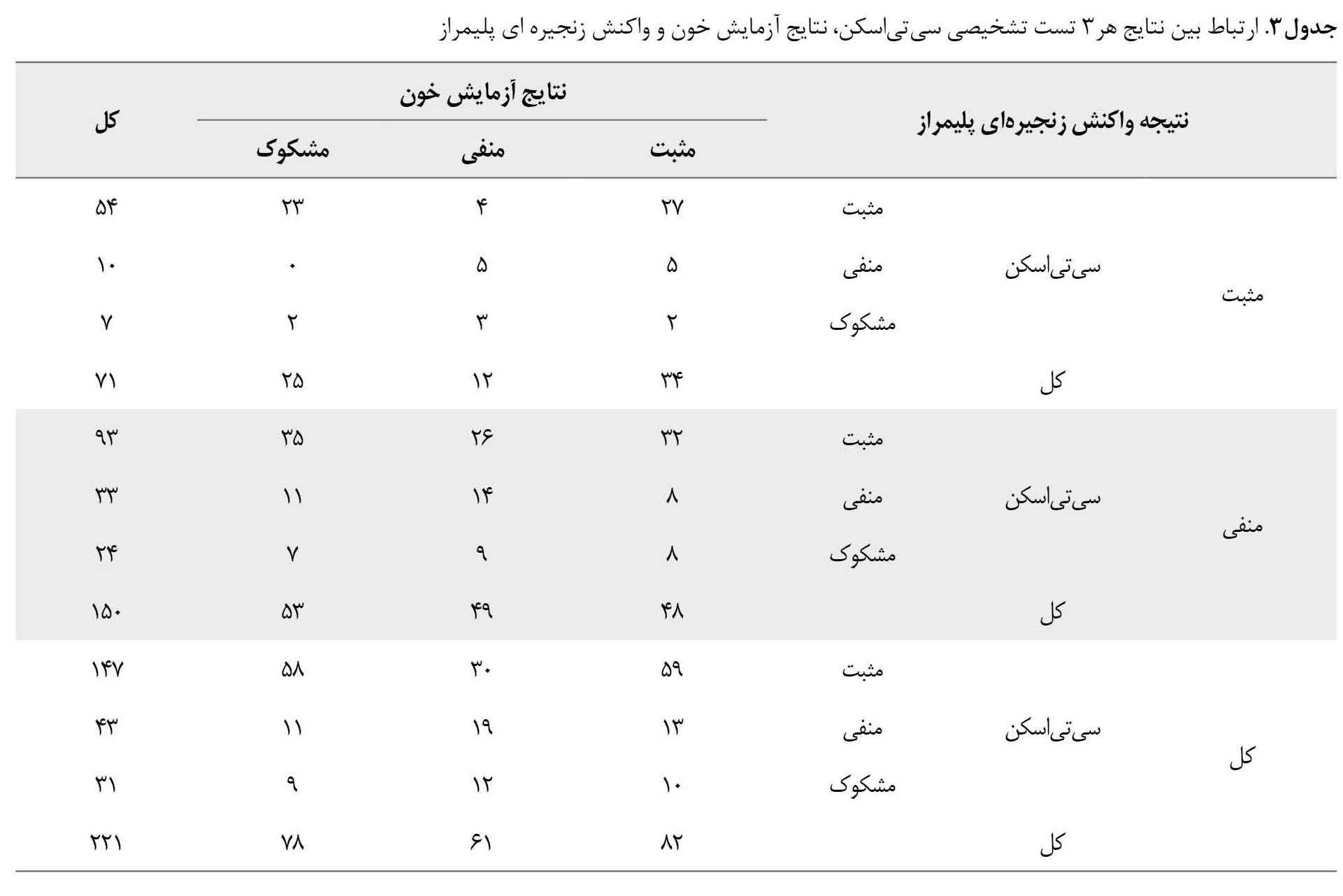
ارتباط معناداری در کسانی که سیتیاسکن، آزمایشات خونی و واکنش زنجیرهای پلیمراز همپای مثبت (هر 3 آیتم مثبت) دارند دیده نشد.
بحث و نتیجهگیری
این پژوهش با هدف بررسی روابط و استفاده از نتایج سیتیاسکن ریه و آزمایش خون در تأیید یا عدم تأیید نتایج واکنش زنجیرهای پلیمراز همپا انجام شد. آزمایشات خونی در 37/1 درصد از موارد مثبت شد. سیتیاسکن نیز در 66/5 درصد نتایج مثبت نشان داد و نتیجه واکنش زنجیرهای پلیمراز همپا نیز در 32/1 درصد بیماران مثبت شد. ازآنجاکه بیشتر بیماران آلوده به کوویدـ19 دچار ذاتالریه و الگوهای مشخص تصویربرداری سیتیاسکن هستند، معاینات رادیولوژی در تشخیص زودرس و ارزیابی دوره بیماری بسیار مهم و حیاتی است. تا به امروز، یافتههای سیتیاسکن بهعنوان شواهد اصلی برای تشخیص بالینی کوویدـ19 در هوبی چین و اکثر کشورهای جهان توصیه شده است [18].
متغیرهای سیتیاسکن و آزمایش خون دارای 3 سطح مثبت، منفی و مشکوک هستند و نتایج آزمایش واکنش زنجیرهای پلیمراز همپا دارای 2 سطح مثبت و منفی است. طبق نتایج پژوهش حاضر، میزان حساسیت اولیه سیتیاسکن برابر 66/5 درصد، آزمایشات خونی 37/1 درصد و واکنش زنجیرهای پلیمراز همپا به میزان 32/1 درصد بود که نصراللهزاده و همکاران (1399) در پژوهش خود میزان 69 درصد و 89 درصد را به ترتیب برای موارد واکنش زنجیرهای پلیمراز همپا و سیتیاسکن مثبت ذکر کردند [19]. مطالعه فانگ نیز در ابتدای بیماری میزان واکنش زنجیرهای پلیمراز مثبت را 71 درصد نسبت به 98 درصد نتایج مثبت سیتیاسکن، ذکر کرد [20]. همچنین این نسبت در پژوهش 88تائو آی درصد به 59 درصد بیان شد [21]. این یافتهها میتوانند به اهمیت انجام سیتیاسکن در اوایل بیماری با وجود علائم اولیه بالینی اشاره کنند. گرچه تفاوت در درصدهای ذکرشده میتواند به دلیل تفاوتهای تشخیصی، خطاهای انسانی و همچنین تفاوت در انواع تستهای واکنش زنجیرهای پلیمراز همپا باشد.
همچنین در مطالعه ذکرشده، در 75 درصد بیماران با واکنش زنجیرهای پلیمراز منفی، نتایج سیتیاسکن مثبت بود [21] که در پژوهش ما نیز باتوجهبه اینکه از 150 نفر با واکنش زنجیرهای پلیمراز منفی، 93 نفر علائم مثبتی در سیتیاسکن خود داشتند، این میزان 62 درصد گزارش شد. برخی مطالعات موردی نیز [22] نشان میدهند بیماران در بدو ورود میتوانند بدون علائم در آزمایشات خونی و با واکنش زنجیرهای پلیمراز منفی، یافتههای مثبتی از سیتیاسکن به نفع کوویدـ19 داشته باشند که تأکیدی مجدد بر اهمیت بیشتر نتایج سیتیاسکن است.
از تمام 221 نفر فقط در 27 نفر (12 درصد) نتیجه هر 3 ابزار تشخیصی مثبت بوده است که احتمالا این مسئله وابسته به شدت بیماری نیز خواهد بود که مورد بررسی قرار نگرفت. همچنین در این مطالعه 76 درصد از بیماران با واکنش زنجیرهای پلیمراز مثبت، علائم مثبتی نیز در سیتیاسکن خود داشتند که این میزان در مطالعه شو و همکاران 72 درصد گزارش شد [15]. اگرچه در برخی مطالعات این میزان 100 درصد نیز گزارش شده است [11، 23]. علائم سیتیاسکن در کودکان نیز مشابه بزرگسالان میتواند وجود داشته باشد، بهطوریکه با وجود واکنش زنجیرهای پلیمراز، لکوپنی و لنفوسیتوپنی مثبت تنها در یکسوم کودکان، سیتیاسکن مثبت بود [24].
همچنین در مطالعه حاضر 47/8 درصد از افراد با واکنش زنجیرهای پلیمراز مثبت، دادههایی به نفع بیماری در آزمایشات خونی خود داشتند که این میزان به طور میانگین در مطالعات دیگر 56 درصد [23] و 63 درصد [11] گزارش شده است. در مطالعه گوان [8] نیز این میزان 83/2 درصد عنوان شده که البته تنها مربوط به لنفوسیتوپنی است. اگرچه یافتههایی نیز مبنی عدم تغییر لنفوسیتها در روزهای اولیه بیماری وجود دارد [25].
در 14 نفر (6 درصد) از نمونههای موردپژوهش، هر 3 تست منفی بوده که میتواند به دلایل خطای تشخیص پزشکی یا بیماریهای با علائم ظاهری مشابه باشد. اگرچه باتوجهبه نوع مطالعه حاضر (گذشتهنگر)، عدم امکان بررسی سریال هرکدام از این تستهای تشخیصی در این مطالعه میتواند جزء محدودیتهای آن به شمار آید. درنهایت حدود 14 درصد علیرغم داشتن آزمایش خون و سیتیاسکن ریه مثبت، واکنش زنجیرهای پلیمراز منفی داشتند که میتواند به اهمیت زمان مناسب انجام تست واکنش زنجیرهای پلیمراز و حذف علل منفی شدن کاذب اشاره کند.
باتوجهبه سهولت دسترسی و نتایج سریع اسکنرهای سیتی در مقایسه با کیتهای واکنش زنجیرهای پلیمراز همپا، تصویربرداری سیتی در خط مقدم ابزارهای غربالگری کوویدـ19 قرار دارد. تصویربرداری با استفاده از سیتی نقش مهمی در تشخیص کوویدـ19 خصوصاً در مراحل اولیه بیماری (بار ویروسی کم) دارد، این در حالی است که آزمایش سواب، ممکن است منفی باشد. علاوهبراین تفاوتهای زیاد در نتایج بهدستآمده از نمونههای واکنش زنجیرهای پلیمراز بینی، حلق، برونش و غیره و همچنین شرایط استاندارد ویژه برای نگهداری، انتقال،کشت و فاصله میان نمونهگیری تا نتیجه [26] نیاز به فرایند منظمی جهت تشخیص صحیح و بهموقع دارد.
باتوجهبه نوع مطالعه حاضر که بهصورت گذشتهنگر انجام شد، امکان بررسی و ثبت سایر علائم بیماران و همچنین انجام سریالی آزمایش واکنش زنجیرهای پلیمراز همپا و سیتیاسکن ریه جهت تعیین دقیقتر حساسیت این فرایندهای تشخیصی وجود نداشت که از محدودیتهای این پژوهش به شمار میرود. پیشنهاد میشود جهت دسترسی به اطلاعات بیشتر و امکان تکرار در انجام آزمایشات خونی و دیگر فرایندهای تشخیصی، این پژوهش بهصورت جاری و آیندهنگر انجام شود.
شناسایی قطعی بیماران مبتلا به کوویدـ19 باتوجهبه شیوع سریع این ویروس میتواند به درمان سریعتر مبتلایان کمک کند. باتوجهبه اینکه جواب آزمایشات خون و واکنش زنجیرهای پلیمراز به دلیل بار کم ویروس در ابتدای بیماری، ممکن است منفی بوده و در صورت وجود علائم مثبت در سایر اقدامات تشخیصی نیاز به تکرار داشته باشند، پیشنهاد میشود همکاران محترم از روی شدت علائم بیماری علاوهبر اخذ و ارسال بلافاصله تست واکنش زنجیرهای پلیمراز و آزمایشات خون به دلیل فاصله زمانی تا حصول نتیجه، سایر اقدامات تشخیصی نظیر سیتیاسکن ریه را در روند کار قرار دهند. گاه نتایج مثبت تست واکنش زنجیرهای پلیمراز بهعنوان تشخیص قطعی کوویدـ19، بعد از فوت بیماران و خاکسپاری آنها به دست همکاران میرسد که نهتنها در تصمیمگیری نهایی کارایی نداشته، بلکه حتی در رعایت پروتکلهای دفن بهداشتی جسد نیز کاربرد نخواهد داشت.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه دارای تأییدیه اخلاقی به شماره IR.MUMS.REC.1399.203از دانشگاه علومپزشکی مشهد است.
حامی مالی
این مقاله منتج از طرح تحقیقاتی مصوب شماره 990255 با حمایت مالی معاونت تحقیقات دانشگاه علومپزشکی مشهد انجام شده است.
مشارکت نویسندگان
تدوین پروپوزال و ثبت طرح پژوهشی: امین ایراندوست و بهاره پایور؛ تجزیهوتحلیل: وحید حاجعلی؛ نمونهگیری و مطالعه علمی پروندهها: امین ایراندوست و محبوبه بهنژاد؛ تدوین و سابمیت مقاله: حمید بزازکاهانی.
تعارض منافع
بنابر اظهار نویسندگان این پژوهش تعارض منافع ندارد.
تشکر و قدردانی
در پایان از مساعدت دانشگاه علومپزشکی مشهد بهخصوص معاونت پژوهشی(کد طرح 990225) بهخاطر تأمین بودجه طرح تحقیقاتی، ریاست، مدیریت محترم، سرپرستاران و کلیه پرسنل بخشهای درمانی و اداری بیمارستان موسی بن جعفر(ع) قوچان کمال تشکر را داریم.
اخیراً شیوع ذاتالریه ویروسی (کوویدـ19) نگرانی جهانی را برانگیخته است. این ویروس برای اولینبار در دسامبر 2019 در استان ووهان چین گزارش شد و سپس بهسرعت در سایر نواحی چین منتشر شده و باعث یک اپیدمی بزرگ با تعداد 80894 مورد ابتلا شامل 3237 مورد مرگ تا هفدهم مارس 2020 شد [1]. در ایران بهطور رسمی در اواخر بهمن 1398 اولین موارد ابتلا به این ویروس اعلام شد که شامل 43 مورد ابتلا به همراه 8 مورد مرگ بود [2]. طبق آمار رسمی سایت سازمان بهداشت جهانی تا تاریخ 6 اکتبر 2022، برابر با 14 مهرماه 1401، تعداد کل موارد ابتلا در دنیا 625129794 مورد بوده است که از این تعداد 6556063 مورد جان خود را از دست دادهاند [3]. کروناویروس جدید با قدرت عفونتزایی بالا که بهطور رسمی Sever Acute Respiratory Syndrome Coronavirus2 و بهاختصارا SARSCoV-2 نامیده میشود، متعاقباً بهواسطه بررسی توالی ژنی و مطالعات اتیولوژیک بهعنوان عامل پاتوژن این شیوع گسترده معرفی شد [4 ,5]. باتوجهبه ماهیت عفونتزایی شدید این بیماری و فقدان استراتژیهای درمانی و دارویی اثباتشده و همچنین عدم کشف واکسن مؤثر تاکنون [6, 7] تشخیص سریع و قطعی در مراحل اولیه بروز بیماری از اهمیت حیاتی برخوردار است. تشخیص بیماری کوویدـ19 اساساً بر یافتههای آزمایشگاهی و رادیوگرافیک استوار است. در کل دنیا رادیولوژیستها با تشخیص کوویدـ19 نقش کلیدی در پیشبرد تشخیص و افتراق تظاهرات بالینی این بیماری از سایر یافتههای رادیولوژیک مشابه [8] و همچنین ارزیابی شدت و پیشرفت بیماری [9] دارند. البته روش تشخیصی اصلی که در بیشتر کشورها بهعنوان استاندارد طلایی تشخیصی محسوب میشود، واکنش زنجیرهای پلیمراز همپا بوده که RNA ویروس را شناسایی میکند [10]. تجربه کشورهای درگیر این بیماری حاکی از آن است که سیتیاسکن قفسه سینه میتواند با فراهم کردن جزئیات ویژه ظریف، نقش حیاتی در غربالگری و تشخیص پنومونی داشته باشد. مشخصه برجسته تصاویر رادیولوژیک در بیماران پنومونی در کوویدـ19 نمای شیشه مات و تراکم ریه است که میتواند هر 2 ریه را درگیر کند [8]. براساس تظاهرات بالینی نیز شایعترین علائم بیماری شامل تب، سرفه خشک، خستگی، تنفس کوتاه و سطحی، بیاشتهایی و اختلال در حس چشایی و ضایعات ریه در سیتیاسکن است. با وجود این در برخی از بیماران علائم و مشکلات شدید و حاد مربوط به پنومونی شامل سندرم زجر تنفسی حاد، ادم ریه، آسیب حاد کلیوی و یا نارسایی تعداد زیادی از ارگانهای بدن مشاهده میشود [11، 12].
علاوهبر سیتیاسکن و واکنش زنجیرهای پلیمراز همپا، آزمایشات خونی نظیر افزایش میزان CRP و LDH و همچنین تغییراتی در CBC نظیر لکوپنی یا لنفوسیتوپنی میتواند ما را به تشخیص قطعی نزدیکتر کنند [13]، اما باتوجهبه دوره کمون نامشخص و کاملاً متفاوت [14]، وجود افراد مبتلا به ویروس بدون علامت بالینی [15] و یا داشتن PCR منفی [16]، و علاوهبرآن باعنایت به وجود سیل زیاد اطلاعات رسمی و غیررسمی مبتنی بر پژوهش یا برخلاف آن براساس عقیده و نظر اثباتنشده، نیاز به توسعه و اتکای بر یافتههای مبتنی بر شواهد است تا به ارتقای کیفیت مراقبتهای بهداشتی و درمانی منجر شود [17] . بنابراین نیاز به بررسی بیشتر و مقایسه روشهای موجود و تعیین میزان همسویی بین روشهای رایج تشخیصی ازجمله سیتیاسکن واکنش زنجیرهای پلیمراز همپا و آزمایش خون است.
علی رغم مطالعات نسبتاً زیادی که درزمینه تظاهرات بالینی، رادیوگرافیک و آزمایشگاهی این بیماری تاکنون انجام شده است، مطالعات بسیار محدودی ارتباط بین تست اسمیر حلق، آزمایشگاهی و رادیولوژیک بیماران را مورد بررسی قرار دادهاند. بنابراین باتوجهبه اهمیت فوقحیاتی تشخیص سریع و قطعی این بیماری در درمان و میزان بقای بیماران، در این مطالعه بر آن شدیم تا با بررسی معیارهای آزمایشگاهی، سیتیاسکن ریه و واکنش زنجیرهای پلیمراز همپای بیماران مشکوک و قطعی کوویدـ19 در شهرستان قوچان، میزان تطابق نتایج روشهای روتین سهگانه با یکدیگر را در تشخیص بیماری بررسی کنیم.
مواد و روشها
پژوهش حاضر با کد اخلاق IR.MUMS.REC.1399.203 یک مطالعه گذشتهنگر است که بهمنظور تعیین معیارهای آزمایشگاهی و سیتیاسکن ریه با واکنش زنجیرهای پلیمراز همپا در بیماران مشکوک و قطعی کوویدـ19 در شهرستان قوچان انجام شد. به ملاحظات اخلاقی ازجمله حفظ محرمانگی افراد و گزارشدهی نتایج پژوهش بهصورت کلی توجه شد. جامعه پژوهش کلیه 400 بیمار مشکوک به کوویدـ19 مراجعهکننده به بیمارستان موسی بن جعفر (ع) از اول اسفند 1398 لغایت آخر اردیبهشت 1399 بود که برایشان آزمایش خون و یا سیتیاسکن ریه و بررسی واکنش زنجیرهای پلیمراز همپای حلق در بیمارستان انجام شد و سوابق و مستندات آن موجود است. روش نمونهگیری، بهصورت سرشماری و براساس معیارهای ورود و خروج صورت گرفت. معیارهای ورود به مطالعه: 1. ورود و بستری در بیمارستان با احتمال یا داشتن علائم کرونا و شروع پروسه درمان کوویدـ19 توسط متخصص داخلی یا عفونی؛ 2. انجام هر 3 اقدام پاراکلینیکی (آزمایش خون و سیتیاسکن ریه و واکنش زنجیرهای پلیمراز همپای حلق) برای بیمار در بیمارستان و وجود سوابق و مستندات در بایگانی بیمارستان.
پس از اخذ تاییدیه و کد اخلاق از دانشگاه علومپزشکی مشهد و اخذ اجازه کتبی از مدیریت شبکه بهداشت و درمان قوچان، با مراجعه به بایگانی اسناد بیمارستان، آزمایشگاه و واحد سیتیاسکن بیمارستان، اطلاعات موردنیاز و از قبل مشخصشده که شامل 5 آیتم آزمایشگاهی (WBC – LYMPHOCIT – CRP – LDH – ESR)، ریپورت مکتوب سیتیاسکن ریه توسط رادیولوژیست و نتیجه تست واکنش زنجیرهای پلیمراز همپای حلق موجود در پرونده بیمار بود، ثبت شد.
به این منظور پژوهشگر باسابقه (کارشناس پرستاری)، بهصورت شبانهروزی و در تمام روزهای هفته به بیمارستان موسی بن جعفر (ع) قوچان مراجعه کرد و پرونده تمام بیماران مراجعهکننده (دارای پرونده) را که تشخیص اولیه آنها کوویدـ19 بود (روش سرشماری) را مورد مطالعه قرار داد و اطلاعات خواستهشده را خارج کرد. از حدود 400 نفر اولیه، کسانی که فاقد معیارهای ورود بودند از لیست خارج، و نهایتاً 221 نفر وارد مطالعه شدند و اطلاعات آنها برای تجزیهوتحلیل تحویل کارشناس آمار شد.
ابزار گردآوری دادهها عبارت بود از فرم ساده طراحیشده جهت ورود دادههای ثبتی پرونده بیماران (بستری در بیمارستان موسی بن جعفر (ع) قوچان بهعنوان تنها مرکز پذیرش بیماران کوویدـ19 در شهرستان قوچان)، شامل سن، جنس، نتیجه آزمایشات پنجگانه خون که در مرحله بعد براساس استانداردهای موجود و توسط متخصص عفونی (فوکال پوینت کرونا) بهصورت منفی، مثبت یا مشکوک گزارش میشد؛ گزارش سیتیاسکن ریه توسط رادیولوژیست بهصورت مثبت، منفی یا مشکوک و جواب آزمایش واکنش زنجیرهای پلیمراز همپا بهصورت مثبت یا منفی. نهایتاً دادهها با استفاده از آمار توصیفی و استنباطی، ازجمله آزمون کایاسکوئر و آماره وی کرامر در نرمافزار SPSS نسخه 19 مورد تجزیهوتحلیل قرار گرفت.
یافتهها
میانگین سنی افراد 11/4±60 سال بود. 48/2 درصد مرد و 51/58 درصد از بیماران زن بودند. متغیرهای موردمطالعه ما، نتایج آزمایش واکنش زنجیرهای پلیمراز همپای حلق، نتایج سیتیاسکن ریه و تشخیص پزشک متخصص عفونی براساس نتایج آزمایشات پنجگانه خون است. جدول شماره 1 فراوانی و درصد نتایج 3 متغیر ذکرشده را نشان میدهد.

جدول شماره 2 که شامل جداول توافقی بین سیتیاسکن ـ واکنش زنجیرهای پلیمراز همپا، آزمایش خون ـ واکنش زنجیرهای پلیمراز همپا و آزمایش خون ـ سیتیاسکن است، میزان همسویی بین گزارش رادیولوژیست از سیتیاسکن و نتایج واکنش زنجیرهای پلیمراز همپا، ارتباط بین آزمایش خون و نتایج واکنش زنجیرهای پلیمراز همپا و ارتباط بین آزمایش خون و نتایج سیتیاسکن را نشان میدهد.

براساس نتایج جدول به نظر میرسد بیشتر افراد با واکنش زنجیرهای پلیمراز همپای مثبت، نتیجه سیتیاسکن مثبت هم داشتهاند (76 درصد). گرچه معنادار بودن این مسئله، با استفاده از آزمون کایاسکوئر و نتایج آن (P=0/118)، رد شد. همچنین به نظر میرسد تعدادی از افراد که نتیجه واکنش زنجیرهای پلیمراز همپای مثبت داشتهاند، دارای آزمایش خون مثبت بودهاند (47/8 درصد) که معنادار بودن این مسئله نیز با استفاده از آزمون کایاسکوئر (P=0/02)، تأیید شد و میزان رابطه این 2 متغیر با آماره وی کرامر 0/186 به دست آمد. علاوهبراین یافتهها نشان میدهند بیشتر افراد با نتیجه آزمایش خون مثبت، نتیجه سیتیاسکن مثبت هم داشتهاند (71/9 درصد). معنادار بودن این مسئله نیز با استفاده از آزمون کایاسکوئر (P=0/019)، تأیید شده و میزان رابطه این 2 متغیر در 3 سطح، با آماره وی کرامر 0/231 به دست آمد.
درنهایت جدول شماره 3 نتایج منفی و مثبت هر 3 تست تشخیصی را در کنار هم نشان میدهد.

ارتباط معناداری در کسانی که سیتیاسکن، آزمایشات خونی و واکنش زنجیرهای پلیمراز همپای مثبت (هر 3 آیتم مثبت) دارند دیده نشد.
بحث و نتیجهگیری
این پژوهش با هدف بررسی روابط و استفاده از نتایج سیتیاسکن ریه و آزمایش خون در تأیید یا عدم تأیید نتایج واکنش زنجیرهای پلیمراز همپا انجام شد. آزمایشات خونی در 37/1 درصد از موارد مثبت شد. سیتیاسکن نیز در 66/5 درصد نتایج مثبت نشان داد و نتیجه واکنش زنجیرهای پلیمراز همپا نیز در 32/1 درصد بیماران مثبت شد. ازآنجاکه بیشتر بیماران آلوده به کوویدـ19 دچار ذاتالریه و الگوهای مشخص تصویربرداری سیتیاسکن هستند، معاینات رادیولوژی در تشخیص زودرس و ارزیابی دوره بیماری بسیار مهم و حیاتی است. تا به امروز، یافتههای سیتیاسکن بهعنوان شواهد اصلی برای تشخیص بالینی کوویدـ19 در هوبی چین و اکثر کشورهای جهان توصیه شده است [18].
متغیرهای سیتیاسکن و آزمایش خون دارای 3 سطح مثبت، منفی و مشکوک هستند و نتایج آزمایش واکنش زنجیرهای پلیمراز همپا دارای 2 سطح مثبت و منفی است. طبق نتایج پژوهش حاضر، میزان حساسیت اولیه سیتیاسکن برابر 66/5 درصد، آزمایشات خونی 37/1 درصد و واکنش زنجیرهای پلیمراز همپا به میزان 32/1 درصد بود که نصراللهزاده و همکاران (1399) در پژوهش خود میزان 69 درصد و 89 درصد را به ترتیب برای موارد واکنش زنجیرهای پلیمراز همپا و سیتیاسکن مثبت ذکر کردند [19]. مطالعه فانگ نیز در ابتدای بیماری میزان واکنش زنجیرهای پلیمراز مثبت را 71 درصد نسبت به 98 درصد نتایج مثبت سیتیاسکن، ذکر کرد [20]. همچنین این نسبت در پژوهش 88تائو آی درصد به 59 درصد بیان شد [21]. این یافتهها میتوانند به اهمیت انجام سیتیاسکن در اوایل بیماری با وجود علائم اولیه بالینی اشاره کنند. گرچه تفاوت در درصدهای ذکرشده میتواند به دلیل تفاوتهای تشخیصی، خطاهای انسانی و همچنین تفاوت در انواع تستهای واکنش زنجیرهای پلیمراز همپا باشد.
همچنین در مطالعه ذکرشده، در 75 درصد بیماران با واکنش زنجیرهای پلیمراز منفی، نتایج سیتیاسکن مثبت بود [21] که در پژوهش ما نیز باتوجهبه اینکه از 150 نفر با واکنش زنجیرهای پلیمراز منفی، 93 نفر علائم مثبتی در سیتیاسکن خود داشتند، این میزان 62 درصد گزارش شد. برخی مطالعات موردی نیز [22] نشان میدهند بیماران در بدو ورود میتوانند بدون علائم در آزمایشات خونی و با واکنش زنجیرهای پلیمراز منفی، یافتههای مثبتی از سیتیاسکن به نفع کوویدـ19 داشته باشند که تأکیدی مجدد بر اهمیت بیشتر نتایج سیتیاسکن است.
از تمام 221 نفر فقط در 27 نفر (12 درصد) نتیجه هر 3 ابزار تشخیصی مثبت بوده است که احتمالا این مسئله وابسته به شدت بیماری نیز خواهد بود که مورد بررسی قرار نگرفت. همچنین در این مطالعه 76 درصد از بیماران با واکنش زنجیرهای پلیمراز مثبت، علائم مثبتی نیز در سیتیاسکن خود داشتند که این میزان در مطالعه شو و همکاران 72 درصد گزارش شد [15]. اگرچه در برخی مطالعات این میزان 100 درصد نیز گزارش شده است [11، 23]. علائم سیتیاسکن در کودکان نیز مشابه بزرگسالان میتواند وجود داشته باشد، بهطوریکه با وجود واکنش زنجیرهای پلیمراز، لکوپنی و لنفوسیتوپنی مثبت تنها در یکسوم کودکان، سیتیاسکن مثبت بود [24].
همچنین در مطالعه حاضر 47/8 درصد از افراد با واکنش زنجیرهای پلیمراز مثبت، دادههایی به نفع بیماری در آزمایشات خونی خود داشتند که این میزان به طور میانگین در مطالعات دیگر 56 درصد [23] و 63 درصد [11] گزارش شده است. در مطالعه گوان [8] نیز این میزان 83/2 درصد عنوان شده که البته تنها مربوط به لنفوسیتوپنی است. اگرچه یافتههایی نیز مبنی عدم تغییر لنفوسیتها در روزهای اولیه بیماری وجود دارد [25].
در 14 نفر (6 درصد) از نمونههای موردپژوهش، هر 3 تست منفی بوده که میتواند به دلایل خطای تشخیص پزشکی یا بیماریهای با علائم ظاهری مشابه باشد. اگرچه باتوجهبه نوع مطالعه حاضر (گذشتهنگر)، عدم امکان بررسی سریال هرکدام از این تستهای تشخیصی در این مطالعه میتواند جزء محدودیتهای آن به شمار آید. درنهایت حدود 14 درصد علیرغم داشتن آزمایش خون و سیتیاسکن ریه مثبت، واکنش زنجیرهای پلیمراز منفی داشتند که میتواند به اهمیت زمان مناسب انجام تست واکنش زنجیرهای پلیمراز و حذف علل منفی شدن کاذب اشاره کند.
باتوجهبه سهولت دسترسی و نتایج سریع اسکنرهای سیتی در مقایسه با کیتهای واکنش زنجیرهای پلیمراز همپا، تصویربرداری سیتی در خط مقدم ابزارهای غربالگری کوویدـ19 قرار دارد. تصویربرداری با استفاده از سیتی نقش مهمی در تشخیص کوویدـ19 خصوصاً در مراحل اولیه بیماری (بار ویروسی کم) دارد، این در حالی است که آزمایش سواب، ممکن است منفی باشد. علاوهبراین تفاوتهای زیاد در نتایج بهدستآمده از نمونههای واکنش زنجیرهای پلیمراز بینی، حلق، برونش و غیره و همچنین شرایط استاندارد ویژه برای نگهداری، انتقال،کشت و فاصله میان نمونهگیری تا نتیجه [26] نیاز به فرایند منظمی جهت تشخیص صحیح و بهموقع دارد.
باتوجهبه نوع مطالعه حاضر که بهصورت گذشتهنگر انجام شد، امکان بررسی و ثبت سایر علائم بیماران و همچنین انجام سریالی آزمایش واکنش زنجیرهای پلیمراز همپا و سیتیاسکن ریه جهت تعیین دقیقتر حساسیت این فرایندهای تشخیصی وجود نداشت که از محدودیتهای این پژوهش به شمار میرود. پیشنهاد میشود جهت دسترسی به اطلاعات بیشتر و امکان تکرار در انجام آزمایشات خونی و دیگر فرایندهای تشخیصی، این پژوهش بهصورت جاری و آیندهنگر انجام شود.
شناسایی قطعی بیماران مبتلا به کوویدـ19 باتوجهبه شیوع سریع این ویروس میتواند به درمان سریعتر مبتلایان کمک کند. باتوجهبه اینکه جواب آزمایشات خون و واکنش زنجیرهای پلیمراز به دلیل بار کم ویروس در ابتدای بیماری، ممکن است منفی بوده و در صورت وجود علائم مثبت در سایر اقدامات تشخیصی نیاز به تکرار داشته باشند، پیشنهاد میشود همکاران محترم از روی شدت علائم بیماری علاوهبر اخذ و ارسال بلافاصله تست واکنش زنجیرهای پلیمراز و آزمایشات خون به دلیل فاصله زمانی تا حصول نتیجه، سایر اقدامات تشخیصی نظیر سیتیاسکن ریه را در روند کار قرار دهند. گاه نتایج مثبت تست واکنش زنجیرهای پلیمراز بهعنوان تشخیص قطعی کوویدـ19، بعد از فوت بیماران و خاکسپاری آنها به دست همکاران میرسد که نهتنها در تصمیمگیری نهایی کارایی نداشته، بلکه حتی در رعایت پروتکلهای دفن بهداشتی جسد نیز کاربرد نخواهد داشت.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این مطالعه دارای تأییدیه اخلاقی به شماره IR.MUMS.REC.1399.203از دانشگاه علومپزشکی مشهد است.
حامی مالی
این مقاله منتج از طرح تحقیقاتی مصوب شماره 990255 با حمایت مالی معاونت تحقیقات دانشگاه علومپزشکی مشهد انجام شده است.
مشارکت نویسندگان
تدوین پروپوزال و ثبت طرح پژوهشی: امین ایراندوست و بهاره پایور؛ تجزیهوتحلیل: وحید حاجعلی؛ نمونهگیری و مطالعه علمی پروندهها: امین ایراندوست و محبوبه بهنژاد؛ تدوین و سابمیت مقاله: حمید بزازکاهانی.
تعارض منافع
بنابر اظهار نویسندگان این پژوهش تعارض منافع ندارد.
تشکر و قدردانی
در پایان از مساعدت دانشگاه علومپزشکی مشهد بهخصوص معاونت پژوهشی(کد طرح 990225) بهخاطر تأمین بودجه طرح تحقیقاتی، ریاست، مدیریت محترم، سرپرستاران و کلیه پرسنل بخشهای درمانی و اداری بیمارستان موسی بن جعفر(ع) قوچان کمال تشکر را داریم.
References
1.Xiong Y, Liu Y, Cao L, Wang D, Guo M, Jiang A, et al. Transcriptomic characteristics of bronchoalveolar lavage fluid and peripheral blood mononuclear cells in COVID-19 patients. Emerg Microbes Infect. 2020; 9(1):761-70. [DOI:10.1080/22221751.2020.1747363] [PMID] [PMCID]
2.Tuite AR, Bogoch II, Sherbo R, Watts A, Fisman D, Khan K. Estimation of coronavirus disease 2019 (COVID-19) burden and potential for international dissemination of infection from Iran. Ann Intern Med. 2020; 172(10):699-701. [DOI:10.7326/M20-0696] [PMID] [PMCID]
3.WHO. WHO Coronavirus Disease (COVID-19) Dashboard [Internet]. 2020 [Updated 2020 October 29]. Available from: [Link]
4.Zhou P, Yang XL, Wang XG, Hu B, Zhang L, Zhang W, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020; 579(7798):270-3. [DOI:10.1038/s41586-020-2012-7] [PMID] [PMCID]
5.Wu F, Zhao S, Yu B, Chen YM, Wang W, Song ZG, et al. Author correction: A new coronavirus associated with human respiratory disease in China. Nature. 2020; 580(7803):E7. [DOI:10.1038/s41586-020-2202-3] [PMID] [PMCID]
6.El Zowalaty ME, Järhult JD. From SARS to COVID-19: A previously unknown SARS- related coronavirus (SARS-CoV-2) of pandemic potential infecting humans - Call for a One Health approach. One Health. 2020; 9:100124. [DOI:10.1016/j.onehlt.2020.100124] [PMID] [PMCID]
7.Torkian P, Ramezani N, Kiani P, Bax MR, Akhlaghpoor S. Common CT findings of novel coronavirus disease 2019 (COVID-19): A case series. Cureus. 2020; 12(3):e7434. [DOI:10.7759/cureus.7434] [PMID] [PMCID]
8.Eastin C, Eastin T. Clinical characteristics of coronavirus disease 2019 in China: Guan W, Ni Z, Hu Y, et al. N Engl J Med. 2020 Feb 28 [Online ahead of print] DOI: 10.1056/NEJMoa2002032. J Emerg Med. 2020; 58(4):711–2. [DOI:10.1016/j.jemermed.2020.04.004] [PMCID]
9.Kooraki S, Hosseiny M, Myers L, Gholamrezanezhad A. Coronavirus (COVID-19) outbreak: What the department of radiology should know. J Am Coll Radiol. 2020; 17(4):447-51. [DOI:10.1016/j.jacr.2020.02.008] [PMID] [PMCID]
10.Wu YC, Chen CS, Chan YJ. The outbreak of COVID-19: An overview. J Chin Med Assoc. 2020; 83(3):217-20. [DOI:10.1097/JCMA.0000000000000270] [PMID] [PMCID]
11.Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020; 395(10223):497-506. [DOI:10.1016/S0140-6736(20)30183-5] [PMID]
12.Chen N, Zhou M, Dong X, Qu J, Gong F, Han Y, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: A descriptive study. Lancet. 2020; 395(10223):507-13. [DOI:10.1016/S0140-6736(20)30211-7] [PMID]
13.Karimi A, Tabatabaei SR, Rajabnejad M, Pourmoghaddas Z, Rahimi H, Armin S, et al. An algorithmic approach to diagnosis and treatment of coronavirus disease 2019 (COVID-19) in children: Iranian expert’s consensus statement. Arch Pediatr Infect Dis. 2020; 8(2):e102400. [DOI:10.5812/pedinfect.102400]
14.Tavakoli A, Vahdat K, Keshavarz M. [Novel coronavirus disease 2019 (COVID-19): An emerging infectious disease in the 21st century (Persian)]. Iran South Med J. 2020; 22(6):432-50. [DOI:10.29252/ismj.22.6.432]
15.Xu X, Yu C, Qu J, Zhang L, Jiang S, Huang D, et al. Imaging and clinical features of patients with 2019 novel coronavirus SARS-CoV-2. Eur J Nucl Med Mol Imaging. 2020; 47(5):1275-80. [DOI:10.1007/s00259-020-04735-9] [PMID] [PMCID]
16.Di Paolo M, Iacovelli A, Olmati F, Menichini I, Oliva A, Carnevalini M, et al. False-negative RT-PCR in SARS-CoV-2 disease: Experience from an Italian COVID-19 unit. ERJ Open Res. 2020; 6(2):00324-2020. [DOI:10.1183/23120541.00324-2020] [PMID] [PMCID]
17.Baghcheghi N, Koohestani HR, Mesri M, Karimi M. [The need to pay attention to evidence-based medicine (EBM) in the diagnosis and treatment of COVID-19 disease (Persian)]. J Arak Univ Med Sci. 2020; 23(5):580-3. [DOI:10.32598/JAMS.23.COV.78.3]
18.Zu ZY, Jiang MD, Xu PP, Chen W, Ni QQ, Lu GM, et al. Coronavirus disease 2019 (COVID-19): A perspective from China. Radiology. 2020; 296(2):E1525. [DOI:10.1148/radiol.2020200490] [PMID] [PMCID]
19.Nasrollahzadeh Sabet M, Khanalipour M, Gholami M, Sarli A, Rahimi Khorrami A, Esmaeilzadeh E. [Prevalence, clinical manifestation and mortality rate in COVID-19 patients with underlying diseases (Persian)]. J Arak Univ Med Sci. 2020; 23(5):740-9. [DOI:10.32598/JAMS.23.COV.5797.1]
20.Fang Y, Zhang H, Xie J, Lin M, Ying L, Pang P, et al. Sensitivity of chest ct for COVID-19: Comparison to RT-PCR. Radiology. 2020; 296(2):E115-7. [DOI:10.1148/radiol.2020200432] [PMID] [PMCID]
21.Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. Correlation of chest CT and RT-PCR testing for coronavirus disease 2019 (COVID-19) in China: A report of 1014 cases. Radiology. 2020; 296(2):E32-40. [DOI:10.1148/radiol.2020200642] [PMID] [PMCID]
22.Huang P, Liu T, Huang L, Liu H, Lei M, Xu W, et al. Use of chest CT in combination with negative RT-PCR assay for the 2019 novel coronavirus but high clinical suspicion. Radiology. 2020; 295(1):22-3. [DOI:10.1148/radiol.2020200330] [PMID] [PMCID]
23.Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020; 323(11):1061-9. [DOI:10.1001/jama.2020.1585] [PMID] [PMCID]
24.Rahimzadeh G, Ekrami Noghabi M, Kadkhodaei Elyaderani F, Navaeifar MR, Enayati AA, Manafi Anari A, et al. COVID-19 infection in Iranian children: A case series of 9 patients. J Pediatr Rev 2020; 8(2):139-44. [DOI:10.32598/jpr.8.2.139]
25.Li T, Lu H, Zhang W. Clinical observation and management of COVID-19 patients. Emerg Microbes Infect. 2020; 9(1):687-90. [DOI:10.1080/22221751.2020.1741327] [PMID] [PMCID]
26.Loeffelholz MJ, Tang YW. Laboratory diagnosis of emerging human coronavirus infections - the state of the art. Emerg Microbes Infect. 2020; 9(1):747-56. [DOI:10.1080/22221751.2020.1745095] [PMID] [PMCID]
1.Xiong Y, Liu Y, Cao L, Wang D, Guo M, Jiang A, et al. Transcriptomic characteristics of bronchoalveolar lavage fluid and peripheral blood mononuclear cells in COVID-19 patients. Emerg Microbes Infect. 2020; 9(1):761-70. [DOI:10.1080/22221751.2020.1747363] [PMID] [PMCID]
2.Tuite AR, Bogoch II, Sherbo R, Watts A, Fisman D, Khan K. Estimation of coronavirus disease 2019 (COVID-19) burden and potential for international dissemination of infection from Iran. Ann Intern Med. 2020; 172(10):699-701. [DOI:10.7326/M20-0696] [PMID] [PMCID]
3.WHO. WHO Coronavirus Disease (COVID-19) Dashboard [Internet]. 2020 [Updated 2020 October 29]. Available from: [Link]
4.Zhou P, Yang XL, Wang XG, Hu B, Zhang L, Zhang W, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020; 579(7798):270-3. [DOI:10.1038/s41586-020-2012-7] [PMID] [PMCID]
5.Wu F, Zhao S, Yu B, Chen YM, Wang W, Song ZG, et al. Author correction: A new coronavirus associated with human respiratory disease in China. Nature. 2020; 580(7803):E7. [DOI:10.1038/s41586-020-2202-3] [PMID] [PMCID]
6.El Zowalaty ME, Järhult JD. From SARS to COVID-19: A previously unknown SARS- related coronavirus (SARS-CoV-2) of pandemic potential infecting humans - Call for a One Health approach. One Health. 2020; 9:100124. [DOI:10.1016/j.onehlt.2020.100124] [PMID] [PMCID]
7.Torkian P, Ramezani N, Kiani P, Bax MR, Akhlaghpoor S. Common CT findings of novel coronavirus disease 2019 (COVID-19): A case series. Cureus. 2020; 12(3):e7434. [DOI:10.7759/cureus.7434] [PMID] [PMCID]
8.Eastin C, Eastin T. Clinical characteristics of coronavirus disease 2019 in China: Guan W, Ni Z, Hu Y, et al. N Engl J Med. 2020 Feb 28 [Online ahead of print] DOI: 10.1056/NEJMoa2002032. J Emerg Med. 2020; 58(4):711–2. [DOI:10.1016/j.jemermed.2020.04.004] [PMCID]
9.Kooraki S, Hosseiny M, Myers L, Gholamrezanezhad A. Coronavirus (COVID-19) outbreak: What the department of radiology should know. J Am Coll Radiol. 2020; 17(4):447-51. [DOI:10.1016/j.jacr.2020.02.008] [PMID] [PMCID]
10.Wu YC, Chen CS, Chan YJ. The outbreak of COVID-19: An overview. J Chin Med Assoc. 2020; 83(3):217-20. [DOI:10.1097/JCMA.0000000000000270] [PMID] [PMCID]
11.Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020; 395(10223):497-506. [DOI:10.1016/S0140-6736(20)30183-5] [PMID]
12.Chen N, Zhou M, Dong X, Qu J, Gong F, Han Y, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: A descriptive study. Lancet. 2020; 395(10223):507-13. [DOI:10.1016/S0140-6736(20)30211-7] [PMID]
13.Karimi A, Tabatabaei SR, Rajabnejad M, Pourmoghaddas Z, Rahimi H, Armin S, et al. An algorithmic approach to diagnosis and treatment of coronavirus disease 2019 (COVID-19) in children: Iranian expert’s consensus statement. Arch Pediatr Infect Dis. 2020; 8(2):e102400. [DOI:10.5812/pedinfect.102400]
14.Tavakoli A, Vahdat K, Keshavarz M. [Novel coronavirus disease 2019 (COVID-19): An emerging infectious disease in the 21st century (Persian)]. Iran South Med J. 2020; 22(6):432-50. [DOI:10.29252/ismj.22.6.432]
15.Xu X, Yu C, Qu J, Zhang L, Jiang S, Huang D, et al. Imaging and clinical features of patients with 2019 novel coronavirus SARS-CoV-2. Eur J Nucl Med Mol Imaging. 2020; 47(5):1275-80. [DOI:10.1007/s00259-020-04735-9] [PMID] [PMCID]
16.Di Paolo M, Iacovelli A, Olmati F, Menichini I, Oliva A, Carnevalini M, et al. False-negative RT-PCR in SARS-CoV-2 disease: Experience from an Italian COVID-19 unit. ERJ Open Res. 2020; 6(2):00324-2020. [DOI:10.1183/23120541.00324-2020] [PMID] [PMCID]
17.Baghcheghi N, Koohestani HR, Mesri M, Karimi M. [The need to pay attention to evidence-based medicine (EBM) in the diagnosis and treatment of COVID-19 disease (Persian)]. J Arak Univ Med Sci. 2020; 23(5):580-3. [DOI:10.32598/JAMS.23.COV.78.3]
18.Zu ZY, Jiang MD, Xu PP, Chen W, Ni QQ, Lu GM, et al. Coronavirus disease 2019 (COVID-19): A perspective from China. Radiology. 2020; 296(2):E1525. [DOI:10.1148/radiol.2020200490] [PMID] [PMCID]
19.Nasrollahzadeh Sabet M, Khanalipour M, Gholami M, Sarli A, Rahimi Khorrami A, Esmaeilzadeh E. [Prevalence, clinical manifestation and mortality rate in COVID-19 patients with underlying diseases (Persian)]. J Arak Univ Med Sci. 2020; 23(5):740-9. [DOI:10.32598/JAMS.23.COV.5797.1]
20.Fang Y, Zhang H, Xie J, Lin M, Ying L, Pang P, et al. Sensitivity of chest ct for COVID-19: Comparison to RT-PCR. Radiology. 2020; 296(2):E115-7. [DOI:10.1148/radiol.2020200432] [PMID] [PMCID]
21.Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. Correlation of chest CT and RT-PCR testing for coronavirus disease 2019 (COVID-19) in China: A report of 1014 cases. Radiology. 2020; 296(2):E32-40. [DOI:10.1148/radiol.2020200642] [PMID] [PMCID]
22.Huang P, Liu T, Huang L, Liu H, Lei M, Xu W, et al. Use of chest CT in combination with negative RT-PCR assay for the 2019 novel coronavirus but high clinical suspicion. Radiology. 2020; 295(1):22-3. [DOI:10.1148/radiol.2020200330] [PMID] [PMCID]
23.Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA. 2020; 323(11):1061-9. [DOI:10.1001/jama.2020.1585] [PMID] [PMCID]
24.Rahimzadeh G, Ekrami Noghabi M, Kadkhodaei Elyaderani F, Navaeifar MR, Enayati AA, Manafi Anari A, et al. COVID-19 infection in Iranian children: A case series of 9 patients. J Pediatr Rev 2020; 8(2):139-44. [DOI:10.32598/jpr.8.2.139]
25.Li T, Lu H, Zhang W. Clinical observation and management of COVID-19 patients. Emerg Microbes Infect. 2020; 9(1):687-90. [DOI:10.1080/22221751.2020.1741327] [PMID] [PMCID]
26.Loeffelholz MJ, Tang YW. Laboratory diagnosis of emerging human coronavirus infections - the state of the art. Emerg Microbes Infect. 2020; 9(1):747-56. [DOI:10.1080/22221751.2020.1745095] [PMID] [PMCID]
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |





